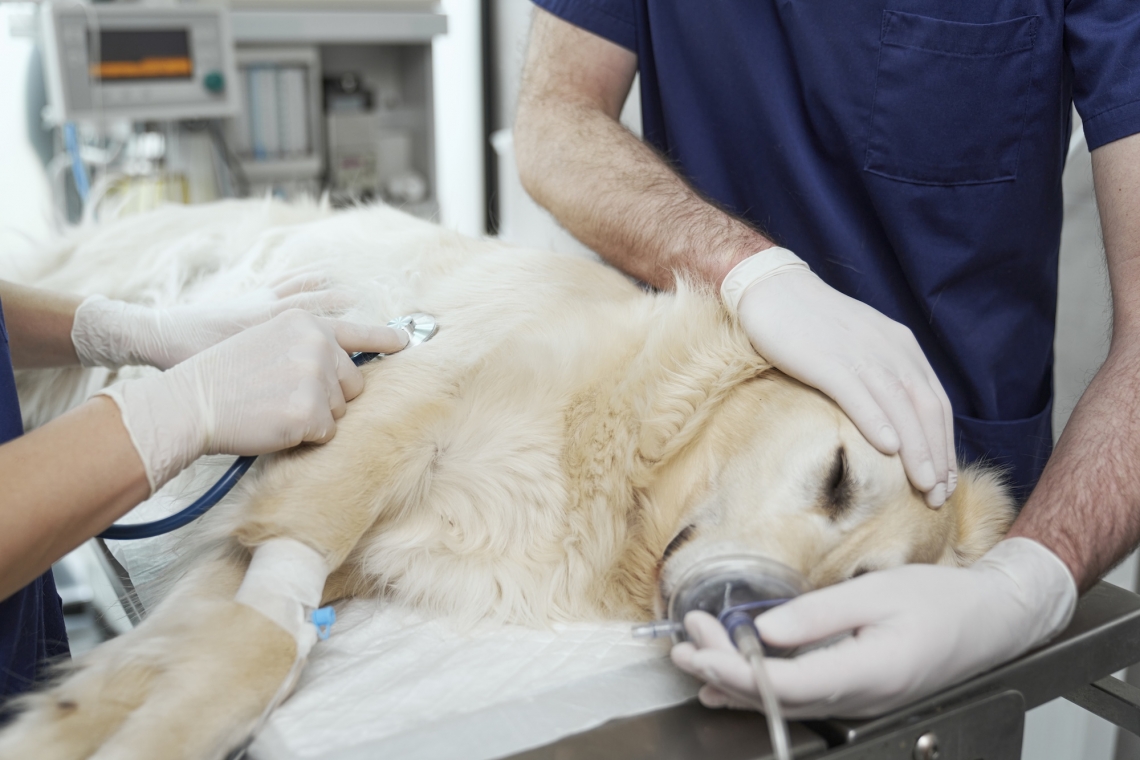
Che cosa è l’emoperitoneo per rottura della milza nel cane ? Per emoperitoneo si intende l’accumulo anomalo di sangue nella cavità peritoneale che può essere determinato da diversi fattori, traumatici e non. Tra le cause non traumatiche, la causa più comune è la neoplasia. Quali sono le cause ed i fattori predisponenti di emoperitoneo da rottura della milza nel cane ? Normalmente risultano colpiti cani adulto-anziani. L' età media dei cani al momento della diagnosi è compresa tra 9 e 11 anni e, al momento, non è stata rilevata alcuna predilezione di sesso. Pastori Tedeschi, Labrador Retriever e Golden Retriever sono razze in cui sono state più frequentemente individuate alcune patologie spleniche (emangiosarcoma ed ematoma splenico) che causano emorragia addominale. Quali sono i principali sintomi clinici dell'emoperitoneo nel cane ? I sintomi clinici di emorragia addominale dipendono dalla gravità dell’emorragia e possono essere essere più o meno gravi causando nel cane da depressione ed abbattimento fino ad un grave shock. E’ anche possibile osservare diminuzione dell’appetito fino ad anoressia completa, addome di volume aumentato (appoggiando la mano sulla parete addominale ed eseguendo una lieve compressione si possono notare movimenti ondulatori della parete), dolore addominale, mucose pallide fino a bianche. In caso di qualunque di questi sintomi è indispensabile portare al più presto il proprio cane da un Veterinario. Come si diagnostica un versamento addominale emorragico nel cane ? Dopo la visita clinica, il veterinario potrà richiedere alcuni esami aggiuntivi come per esempio Radiografie addominali ed eventualmente toraciche, Ecografia addominale, esami Ematologici e se presente un versamento addominale potrà essere richiesto anche l’esame del liquido prelevato. Con questi esami il Medico Veterinario potrà confermare la diagnosi di emorragia addominale ed eventualmente diagnosticare la presenza di neoformazioni che interessano la milza o anche altri organi. E’ possibile sapere se la neoformazione è benigna o maligna prima dell’intervento? Purtroppo no. Diversi studi scientifici hanno cercato un metodo efficace per poter avere una diagnosi pre-operatoria attendibile (esami citologici, esami del versamento addominale, ecografia, Tomografia computerizzata), ma senza risultato. Tali esami diagnosticano molti falsi negativi, sottostimando la diagnosi di neoplasia. L' unico modo per avere la diagnosi di certezza è quella di far analizzare il pezzo anatomico rimosso chirurgicamente mediante esame istologico. Intervento chirurgico Per bloccare l’emorragia da rottura di milza nel cane, il Medico Veterinario potrà decidere di stabilizzare il paziente con terapia appropriata e procedere poi ad intervento chirurgico che ha lo scopo di bloccare l’emorragia, il che, molto spesso, prevedere l’asportazione di tutta la milza, soprattutto se è presente una massa. Durante la chirurgia, inoltre, il Veterinario potrà anche eseguire un controllo di tutti gli organi addominali ed effettuare delle biopsie diagnostiche se si riscontrano reperti anomali (esempio biopsie epatiche se si notano noduli sul fegato). Il cane può vivere senza milza, infatti le funzioni svolte dalla milza saranno sostituite da altri organi. Prognosi dell’emorragia addominale da rottura di milza nel cane La prognosi risulta correlata alla durata dell’emorragia, all’esito della chirurgia e dell’esame istologico. La prognosi potrà essere “favorevole” nel caso in cui la lesione splenica sia benigna o al contrario “riservata” (con tempi ridotti di sopravvivenza) in caso di tumori maligni ed in assenza di chemioterapia post operatoria. Nel caso in cui si dovesse trattare di un tumore maligno, si consiglia sempre un consulto con un veterinario oncologo, per poter discutere al meglio delle possibilità mediche correlate alla diagnosi istologica ed allo stadio della malattia in corso. Medicina preventiva La prevenzione della rottura di milza non traumatica può essere determinante per la sopravvivenza del proprio amico cane. In base alla razza ed età del cane il Medico Veterinario consiglierà lo screening periodico più adatto al fine di individuare ed eventualmente studiare le neoformazioni della milza (Rx, Ecografia, TC, citologia, biopsia) e poter quindi agire tempestivamente.Articolo redatto in collaborazione con la Dr.ssa Elisa Olivieri Medico Veterinario “DVM, Dipl. (ECVS) college europeo di chirurgia, GPcert in Endoscopia., GPCert in Cardiologia"Dr. Vincenzo MontinaroAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Nel gatto, l’aumento della sete (polidipsia) e della produzione urinaria (poliuria) possono essere conseguenti a diverse cause. In questo articolo andremo ad esaminarne alcune tra le cause più frequenti, fornendo inoltre consigli pratici su come gestire il proprio animale in attesa di una diagnosi nonché su come fornire al Medico Veterinario tutte le informazioni necessarie per un rapido inquadramento del problema. Con il termine polidipsia si intende un aumento del volume dei liquidi assunti. La polidipsia può essere il sintomo primario, oppure, più frequentemente, può essere la conseguenza ad un aumento delle perdite di liquidi attraverso la minzione (poliuria). L’incrementata produzione di urine o poliuria è infatti un’importante causa di disidratazione, a cui l’animale risponde bevendo maggiormente. Come posso capire se il mio gatto beve ed urina troppo? Oggettivare se il proprio gatto ha poliuria e/o polidipsia non è semplice. In condizioni normali, il gatto ha la tendenza ad assumere scarse quantità di acqua durante la giornata. Ciò è ancora più vero se viene alimentato principalmente con alimento umido. Se il gatto manifesta un improvviso cambio di abitudini, in termini di aumento del tempo trascorso presso la ciotola o di ricerca di acqua presso rubinetti o sanitari, potrebbe rappresentare il primo segnale di aumento della sete. Per oggettivare il dato, è possibile misurare la quantità di acqua somministrata nell’arco delle 24 ore riempiendo la ciotola facendo uso di una bottiglia o di un qualsiasi contenitore graduato. Se il gatto assume una quantità di acqua > 45 ml/kg in 24 ore (ad es, per un gatto di 5 kg più di 225 ml in 24 h), è indicativo di uno stato di polidipsia. Avere una comprensione più accurata della quantità di acqua consumata semplificherà la valutazione del Medico Veterinario nel rilevare eventuali alterazioni della sete. La misurazione del peso specifico urinario, effettuabile dal Medico Veterinario attraverso un rifrattometro, completerà la valutazione complessiva al fine di confermare la veridicità del sintomo percepito. Infatti, gli aumentati livelli di sete e minzione nei gatti sono comunemente associati a una ridotta concentrazione delle urine. Il sintomo poliuria/polidipsia, nonostante non debba sempre destare preoccupazioni, potrebbe fungere da segnale di allarme riguardo a una potenziale malattia sottostante. Pertanto, il veterinario consiglierà una serie di indagini per individuare la causa sottostante. Ottenere una diagnosi tempestiva può permettere un trattamento rapido, riducendo sia l'intensità della sete che, soprattutto, l'evoluzione della malattia di fondo. Può essere utile ridurre la quantità di acqua a disposizione del mio gatto? Ridurre deliberatamente l’accesso all’acqua da parte del gatto è un comportamento da evitare sempre, poiché può portare a rapida disidratazione dell’animale, con possibili gravi conseguenze. Al contrario, a fronte di un aumento della sete, è necessario garantire sempre il libero accesso all'acqua e rivolgersi prontamente al Medico Veterinario per indagare il problema. Quali sono le principali patologie che portano a poliuria e polidipsia nel gatto? Nella seguente tabella sono riportate le più comuni cause di poliuria e polidipsia nel gatto. Tra di esse troviamo le malattie renali, le malattie ormonali, le malattie del fegato e le anomalie degli elettroliti (sali minerali) nel sangue, che a loro volta riconoscono diverse cause. CAUSE COMUNI DI POLIURIA E POLIDIPSIA NEI GATTI Malattia renale cronica Condizione degenerativa a carico dei reni Diabete mellito Aumentata concentrazione di glucosio nel sangue dovuta ad una carenza nella produzione e/o azione di insulina Ipertiroidismo Aumentata produzione degli ormoni tiroidei Pielonefrite Infezione a carico dei reni Ipercalcemia Aumentata concentrazione di calcio nel sangue, dovuta a malattie ormonali o tumorali, piuttosto che a causa ignota Insufficienza epatica Ridotta funzionalità del fegato, può derivare da diverse patologie epatiche Ipokaliemia Ridotta concentrazione di potassio nel sangue, spesso legata a malattie del rene o dell’intestino Diabete insipido Ridotta produzione e/o azione dell’ormone vasopressina, implicato nel regolare la capacità a concentrare le urine da parte dei reni. Tab. - Malattie più comunemente implicate nell’aumento di sete e minzione del gatto. Le indagini consigliate dal Medico Veterinario saranno personalizzate in base alla storia clinica, all'età e ai risultati della visita generale dell’ animale. Spesso, verranno raccomandate analisi del sangue e delle urine, comprese urinocolture per identificare eventuali batteri responsabili di infezioni urinarie. A seconda dei risultati, potrebbero essere necessari ulteriori esami per individuare anomalie ormonali o problemi di funzionalità epatica. Esami di diagnostica per immagini, come radiografie toraciche o ecografie addominali, potrebbero essere cruciali per una valutazione completa del paziente. Malattia renale cronica Benché possa colpire gatti di ogni età, questa malattia è di riscontro molto frequente nel gatto anziano, colpendo circa 8 gatti su 10 al di sopra dei 15 anni. I reni svolgono un’azione di “filtro” per l’organismo. La loro progressiva degenerazione è seguita da perdita della funzionalità e di conseguenza l’accumulo nel sangue di alcuni cataboliti, ovvero sostanze di scarto normalmente eliminate attraverso le urine. I reni sono inoltre implicati nel bilancio idrico ed elettrolitico. Pertanto, la disfunzione renale comporta la produzione di abbondanti quantità di urine e poco concentrate, cui consegue disidratazione dell’animale, che manifesterà di conseguenza un notevole aumento della sete. Altri sintomi frequenti di malattia renale cronica sono la perdita di peso, la riduzione dell’appetito, la letargia e, negli stadi più avanzati, la comparsa di alitosi e vomito ricorrente. Il Medico Veterinario può efficacemente diagnosticare la malattia renale cronica attraverso la raccolta di una dettagliata storia clinica, la visita generale (comprensiva della misurazione della pressione sistemica), analisi del sangue e delle urine, e l'esecuzione di un'ecografia addominale. Essendo una condizione progressiva e irreversibile, la malattia renale cronica non può essere completamente guaribile. Tuttavia, una diagnosi tempestiva consente di rallentare significativamente la sua progressione mediante opportune modifiche dietetiche e trattamenti farmacologici. Ipertiroidismo Questa malattia è caratteristica del gatto adulto/anziano e rappresenta la malattia endocrina più comune del gatto. L’ipertiroidismo è causato dalla presenza di un tumore tiroideo, generalmente benigno, che produce un eccesso di ormoni tiroidei. Questo incremento ormonale provoca diverse conseguenze nei gatti affetti, tra cui aumento della sete e della minzione, eccessivo appetito, progressiva perdita di peso (dimagrimento) e la comparsa di un mantello di aspetto scadente dovuto alla disidratazione. Inoltre, possono manifestarsi alterazioni comportamentali, come irrequietezza ed iperattività, nonché sintomi gastro-intestinali ricorrenti, quali vomito e diarrea. La diagnosi di questa malattia si basa sulla raccolta di una dettagliata storia clinica che il proprietario potrà raccontare e sulla visita generale del Medico Veterinario che potrà effettuare anche la palpazione del collo, la misurazione della pressione sistemica, l'auscultazione cardiaca, oltre all'esecuzione di analisi del sangue e delle urine. In caso di sospetto clinico di ipertiroidismo, il Medico Veterinario consiglierà la misurazione degli ormoni tiroidei nel sangue, necessaria per ottenere la diagnosi. Ottenere la diagnosi di questa malattia è essenziale poiché esistono diverse opzioni terapeutiche in grado di gestire i sintomi o, in alcuni casi, di consentire la completa guarigione del gatto. Nei gatti adulti con una buona prospettiva di vita e in assenza di altre malattie debilitanti, è possibile individuare la localizzazione e le dimensioni del tumore tiroideo attraverso tecniche avanzate di diagnostica per immagini (scintigrafia tiroidea). La radioiodoterapia, che comporta la "distruzione" del tumore mediante l'uso di iodio radioattivo, rappresenta in tali situazioni la terapia preferenziale, portando a una risoluzione definitiva del quadro nel 95% dei casi. Altre opzioni terapeutiche, come l'intervento chirurgico, la terapia medica o l'adozione di una dieta a basso o nullo contenuto di iodio, potrebbero essere considerate dal Medico Veterinario in base alle caratteristiche specifiche del quadro clinico del gatto. Diabete mellito È la seconda patologia endocrina più comune nel gatto. Alla base di questa endocrinopatia si riscontra una produzione insufficiente di insulina e/o la sua perdita di efficacia, che comportano un aumento dei livelli di glucosio (uno zucchero semplice) nel sangue e nelle urine. La presenza di glucosio nelle urine, definita glicosuria, oltre a predisporre il gatto a possibili infezioni batteriche, provoca la produzione di grandi quantità di urine poco concentrate. In questa situazione, la disidratazione conseguente spinge l'animale a bere in modo eccessivo. Nei gatti diabetici, ulteriori manifestazioni cliniche associate all'aumento della sete e della minzione includono un eccessivo appetito e una progressiva perdita di peso. Nel caso in cui la diagnosi venga ritardata, il diabete mellito potrebbe causare un appoggio anomalo sulle zampe posteriori (plantigradia). L'iter diagnostico, anche in questo contesto, prende avvio dalla racconto scrupoloso dei sintomi, con particolare attenzione alle abitudini alimentari e all'attività fisica del paziente. La visita clinica e le analisi del sangue e delle urine risultano indispensabili per formulare la diagnosi. La presenza di iperglicemia persistente associata a glicosuria, ossia livelli elevati di glucosio rispettivamente nel sangue e nelle urine, rappresenta di per sé la diagnosi di diabete. Inoltre, la misurazione delle fruttosamine, proteine nel sangue che si legano al glucosio durante iperglicemie prolungate, può ulteriormente assistere il Medico Veterinario nella conferma del diabete mellito e fornire strumenti per il monitoraggio terapeutico. Quando il Medico Veterinario avrà confermato la diagnosi di diabete mellito, il gatto dovrà essere trattato con insulina e una dieta apposita. Saranno previsti frequenti monitoraggi clinici e glicemici nella fase iniziale, al fine di stabilire la dose di insulina più appropriata per l’ animale. Riconoscere e trattare tempestivamente il diabete è cruciale, poiché, se trascurato a lungo, questa patologia può evolvere in una condizione d’urgenza nota come chetoacidosi diabetica. Inoltre, è importante sottolineare che, con un tempestivo e corretto approccio terapeutico, il 20-30% dei gatti diabetici può andare incontro a remissione. Cause meno comuni di Poliuria e Polidipsia nel gatto Il sintomo poliuria/polidipsia nel gatto può dipendere anche da altre cause meno comuni. Ad esempio, alcune diete o determinati farmaci possono essere associati a questo sintomo. Pertanto, è opportuno informare il veterinario su tutti i farmaci somministrati di recente (compresi colliri e creme topiche) e fornire una descrizione dettagliata della dieta che sta assumendo l’animale e delle eventuali supplementazioni. Conclusioni Considerate le molteplici cause di aumento della sete e della minzione nel gatto, l’iter diagnostico potrebbe apparire complesso, articolato ed impegnativo dal punto di vista economico. Va tuttavia precisato che normalmente si procede in maniera sequenziale, escludendo dapprima le cause più comuni, che spesso sono già evidenti con esami ematici e urinari di base. Nei casi più complessi si renderanno necessarie indagini più approfondite. È importante sapere che alcuni degli accertamenti diagnostici necessari potrebbero richiedere l'ospedalizzazione dell'animale. Identificare la causa specifica alla base dei sintomi di poliuria e polidipsia nel gatto è nel pieno interesse dell’animale e potrebbe comportare diversi tentativi diagnostici non sempre garantendo una risposta definitiva. Il raggiungimento di una diagnosi e l’impostazione di una terapia adeguata può tuttavia comportare un netto miglioramento nella qualità di vita del proprietario e dell’animale stesso. “DVM, PHD, Diplomata ECVIM-CA, European College of Veterinary Internal Medicine – Companion Animals.Dr.ssa Francesca Del BaldoAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

L’elettrocardiogramma è la registrazione della frequenza e del ritmo cardiaco durante la visita clinica e può avere una durata variabile da alcuni secondi ad un massimo di alcuni minuti.L’esame Holter invece è un metodo non invasivo di valutazione del ritmo e della frequenza cardiaca a domicilio durante un intervallo di tempo molto maggiore, solitamente 24-48 ore. Questa metodica prende il nome dal suo inventore, il fisico statunitense Norman J. nel 1950, e successivamente impiegata in ambito veterinario a partire dagli anni ‘90. Viene proposto un esame Holter quando un paziente (cane o gatto) presenta: Sincopi (eventi transitori di perdita della coscienza) Intolleranza all’esercizio fisico, dopo che il Medico Veterinario ha escluso altre cause ed è stato eseguito un esame ecocardiografico, con il sospetto della presenza di aritmie intermittenti Riscontro di un’aritmia alla visita clinica In presenza di patologie cardiache (come la tachicardia ventricolare ereditaria del pastore tedesco, la malattia aritmogena, la cardiomiopatia dilatativa, l'endocardiosi valvolare, la fibrillazione atriale) Per verificare il corretto funzionamento del pacemaker Valutazione dell’efficacia di una terapia antiaritmica Screening in determinate razze (ad es Boxer e Dobermann) Come avviene la registrazione Holter? Per effettuare il monitoraggio Holter occorre applicare su entrambi i lati del torace dell’animale, previa tricotomia (quindi tosatura del pelo fino alla pelle) e pulizia della zona d’interesse con soluzione alcolica che verrà successivamente debitamente asciugata e fatta evaporare, alcuni specifici elettrodi adesivi. Questi, dopo averne assicurato la tenuta, con dello scotch medicale aggiuntivo, sono connessi tramite appositi cavi al registratore, ovvero una piccola unità digitale che viene posizionata sul dorso del paziente e fissata in sede mediante bendaggio o appositi indumenti dedicati. Tutti i cavi verranno ricoperti da passaggi di cotonina ed altra fasciatura, onde evitare che questi penzolino, correndo il rischio che si stacchino o che siano degli agganci per l’animale durante un normale grattamento, invalidando l’esame. Una volta smontato il dispositivo, attraverso un software dedicato si scaricherà tutta la registrazione ed il Medico Veterinario cardiologo si occuperà della lettura e refertazione dell’esame. Il proprietario dovrà tenere un diario delle principali attività del suo animale per tutto il tempo della registrazione. Ciò sarà fondamentale per l’interpretazione del tracciato. Il vantaggio di questo esame è permettere una registrazione di lunga durata oltre ad essere una metodica assolutamente non invasiva, solitamente estremamente ben tollerata e facile da effettuare. Gli animali normalmente tollerano bene l’applicazione degli elettrodi e del registratore perché, come anticipato, ad oggi esistono numerosi abbigliamenti per animali studiati adeguatamente per questa indagine diagnostica con una tasca atta a contenere il registratore. Ovviamente il proprietario dovrà avere alcune accortezze durante la registrazione, quali ad es evitare di far bagnare il dispositivo (ad esempio portando l’animale in passeggiata sotto la pioggia), evitare di condurre l’animale in luoghi frequentati da altri animali, verificare che il cane non tenda a strapparsi tutto e/o a rotolarsi ripetutamente sulla schiena, eccetera, ma nella maggior parte dei casi non vi è la necessità di alcuna azione eccezionale oltre il buon senso. In copertina - Pettorina copri e porta Holter in un cane. In copertina - Le foto sono gentilmente concesse dagli Autori.“Med. Vet., Med Vet, GPCert in Cardiologia - (Cardiologia)”Dr.ssa Marta ClarettiAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Il criceto è un simpatico roditore di piccola taglia che grazie al suo carattere e alle dimensioni ridotte viene scelto come animale da compagnia. Dobbiamo rispettare le sue esigenze nutrizionali ed allestire un luogo adatto alle sue necessità per farlo vivere in salute.È onnivoro e in natura mangia semi, cereali, larve di insetti e insetti. Come animali domestici, i criceti necessitano di una dieta di buona qualità ed equilibrata che contenga tutti i nutrienti e i minerali di cui hanno bisogno. La razione ideale deve essere composta da un buon pellet e da una miscela di semi del commercio formulata per le necessità della specie, evitando di somministrare semi di girasole, snack contenenti semi di girasole, miele, zuccheri e arachidi, poiché questi prodotti sono spesso contaminati da muffe ed essendo ricchi di grassi favoriscono l’obesità. Gradiscono piccole quantità di insetti (camole del miele e della farina, grilli), pollo cotto non condito, ricotta a basso contenuto di grassi e senza sale, pezzetti di uovo sodo, pane integrale e uova strapazzate. La dieta può essere completata da frutta e verdura fresca, come mele, carote, broccoli e pere, lavate accuratamente per rimuovere qualsiasi contaminazione prima della somministrazione. I nuovi alimenti devono essere inseriti gradualmente poiché i cambiamenti improvvisi possono causare disturbi digestivi. L'uva e il rabarbaro non dovrebbero essere somministrati perché sono tossici per questi animali. Altri alimenti pericolosi per i criceti sono: avocado, semi di mela e d’uva, cioccolato, mandorle, caramelle, patatine, patate crude, foglie di pomodoro, arance, mandarini, limoni, anguria, marmellata, spezie, porri, aglio, cipolle, erba cipollina. Il cibo deve essere fornito due volte al giorno possibilmente una volta al mattino e una alla sera. I criceti hanno bisogno di avere sempre a disposizione acqua fresca e pulita. Come contenitore si utilizza una bottiglia con un tubo di aspirazione senza valvola, quest’ultima deve essere controllata ogni giorno per eventuali perdite o ostruzioni. I criceti non sono in grado di applicare una forte aspirazione e potrebbero avere difficoltà a superare la resistenza del flusso d'acqua nei tradizionali tubi con valvola a sfera. Si deve scegliere un alloggio spazioso, possibilmente a piani, facile da pulire, sicuro per evitare che si possano ferire. Il fondo deve essere ricoperto da segatura non polverosa, oppure da tutolo di mais o trucioli di legno, non si devono utilizzare fondi con rete metallica o di plastica. Il cibo può essere fornito in piccoli piatti di ceramica direttamente sul pavimento della gabbia, si può posizionare del cibo sul fondo per consentire un comportamento naturale di foraggiamento, in questo caso bisogna rimuovere immediatamente qualsiasi cibo avariato o non consumato. L’alloggio deve essere arredato con una piccola casetta utilizzata come tana e dalla classica ruota che garantisce al criceto serenità ed equilibrio emotivo.Le ruote per criceti non dovrebbero essere tolte durante la notte perché i criceti sono animali notturni che preferiscono essere attivi dopo il tramonto. Se si dovessero notare cambiamenti nell'assunzione di acqua e cibo, feci liquide, regione anale imbrattata di feci o urine maleodoranti è necessario prenotare una visita da un veterinario specializzato. “DVM, GPCert medicina e chirurgia degli animali esotici, Responsabile settore Animali non Convenzionali Mylav La Vallonea”Dr. Gustavo PicciAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}
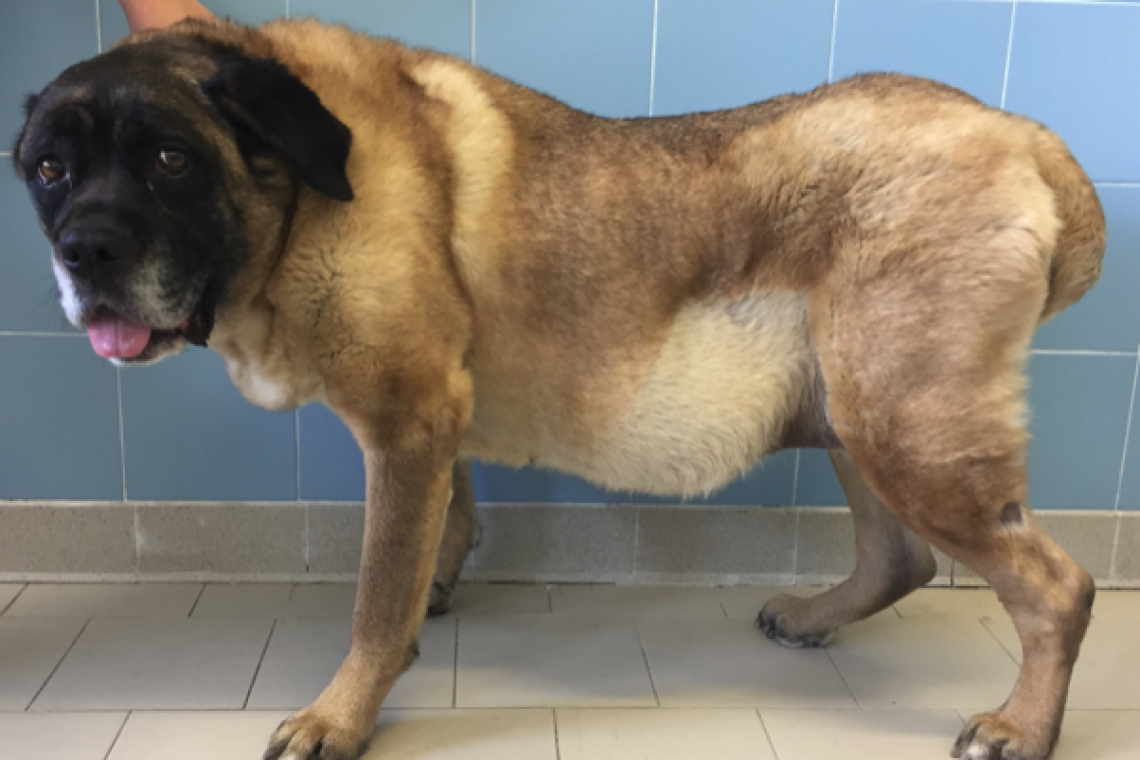
L’aumento di volume dell’addome è un evento che nel cane e nel gatto può riconoscere numerose e diverse cause.In questo articolo andremo a descrivere le principali motivazioni e come riconoscere alcuni sintomi che, associati ad un ingrandimento dell’addome, possono rappresentare un’urgenza medica. L’addome contiene al suo interno diversi organi vitali: lo stomaco, l’intestino, il fegato, la milza, la vescica, i reni, il pancreas, la prostata e l’utero. Alcune malattie a carico di questi organi possono, in certi casi, determinare un aumento di volume dell’addome. Bisogna innanzitutto ricordare che le diverse razze (soprattutto nei cani) possono avere un addome con diverso aspetto: in alcune razze è stretto e alto, in altre appare normalmente più ampio e profondo (FOTO 1).Per poter riconoscere un’eventuale dilatazione addominale è importante ricordare queste importanti differenze di razza. FOTO 1 - Un cane di razza Galgo español (levriero, a destra) e un cane Bovaro del bernese (molossoide, a sinistra).Si può notare come l’ampiezza e la profondità dell’addome sia differente tra le due razze di cani.QUALI SONO LE PRINCIPALI CAUSE DI AUMENTO DI VOLUME DELL’ADDOME? GRAVIDANZA Nel caso più ovvio di un cane o gatto femmina, non sterilizzata, in cui si instaura una gravidanza, si può notare un progressivo aumento di volume dell’addome con il passare delle settimane (FOTO 2).A meno che non sia stato possibile osservare l’avvenuto accoppiamento, cani e gatti con stile di vita prettamente outdoor possono sviluppare una gravidanza inaspettata.FOTO 2 - immagine radiografica dell’addome di una cagna in corso di gravidanza.Le frecce indicano la presenza di alcuni feti, evidenti dai profili delle ossa della colonna vertebrale e della testa.ECCESSO DI ALIMENTI, FECI O PARASSITI NEL TRATTO GASTROENTERICO Un’eccessiva alimentazione, soprattutto in cuccioli o in cani/gatti sottopeso, può causare un transitorio aumento di volume dell’addome che si risolve al termine della digestione. Un accumulo eccessivo di feci nell’intestino può, invece, essere una condizione patologica, come causa o come conseguenza di alcune patologie gastroenteriche (costipazione, megacolon (Leggi), paralisi intestinale). Un’infestazione da parte di parassiti intestinali (solitamente vermi tondi, gli ascaridi), che si sviluppa tipicamente in cuccioli non adeguatamente trattati con farmaci antiparassitari, può determinare la presenza di un addome più dilatato, evidente anche durante il digiuno (FOTO 4).FOTO 4 - addome dilatato in un cucciolo di gatto affetto da un’infestazione di ascaridi (vermi) intestinali. NEOFORMAZIONI IN ADDOME Lo sviluppo di alcuni tumori o neoformazioni negli organi addominali può portare ad un aumento del suo volume. I tumori possono essere di diverso tipo, con diverso comportamento (benigno o maligno) in base all’organo in cui esso si sviluppa e in base alla propria natura. Altri tipi di neoformazioni che si possono sviluppare in addome sono le cisti, delle strutture composte da una capsula che contiene al suo interno un materiale fluido (vedi paragrafo successivo per la natura dei fluidi). Quando queste cisti contengono del pus (fluido composto da globuli bianchi degenerati e batteri) si tratta di una reazione dovuta ad un’infezione, solitamente causata da batteri, e la neoformazione prendono il nome di ascesso. In caso un’infezione cronica (che dura da diverse settimane o mesi) o causata da parassiti, funghi e oggetti solidi che sono penetrati in addome (es. spighe vegetali) si può avere la formazione di granulomi, strutture formate da cellule infiammatorie e tessuto cicatriziale. FLUIDI IN ADDOME In alcuni casi l’addome può aumentare di volume se al suo interno si accumulano dei fluidi patologici. La natura di questi fluidi e le cause del loro accumulo possono essere varie.1) L’accumulo di sangue in addome (emoaddome) è un evento possibile in pazienti che hanno subito un trauma (un investimento, una caduta da altezza elevata) che ha causato la rottura di organi (es. milza o fegato) o di vasi sanguigni.Alcuni tumori, come l’emangiosarcoma (che origina spesso nella milza, un organo addominale estremamente ricco di sangue) possono andare incontro a rottura, anche spontanea senza che vi siano stati traumi, e causare sanguinamenti in addome.Anche l’ingestione accidentale di rodenticidi (sostanze tossiche comunemente utilizzate come esche per topi infestanti) impedisce al sangue di coagulare correttamente, determinando sanguinamenti in addome o in altre parti del corpo. Infine, pazienti che hanno subito una chirurgia addominale possono sviluppare un accumulo di sangue in addome di lieve entità e solitamente non rischioso, che si risolve spontaneamente nei giorni successivi alla chirurgia con le adeguate cure post-operatorie. - Un liquido di natura urinosa (caratterizzato dalla presenza di urina) può riversarsi in addome in seguito alla rottura delle vie urinarie (ureteri, vescica o uretra).- Un liquido di natura biliare (caratterizzato dalla presenza di bile, una sostanza prodotta dal fegato, necessaria per la digestione degli alimenti) può invece essere presente in caso di rottura della cistifellea (l’organo in cui la bile viene immagazzinata). Questi due eventi (rottura delle vie urinarie e delle vie biliari) possono altresì avvenire in seguito ad un trauma o in seguito ad un’ostruzione delle vie specifiche (presenza di calcoli urinari o biliari, tumori che ostruiscono le vie specifiche). - Alcune gravi malattie del fegato (insufficienza epatica, ipertensione epatica) o del cuore (insufficienza cardiaca) possono determinare la formazione di liquidi addominali chiamati trasudati, dei fluidi acquosi con variabili concentrazioni proteiche che originano dal circolo sanguigno.Anche altre malattie croniche es: malattia renale cronica (leggi l'articolo) o enteropatia proteino-disperdente (leggi l'articolo) possono, nei casi più gravi, portare allo sviluppo di questo tipo di fluido in addome. - Quando alcuni organi addominali sviluppano una patologia infiammatoria es. pancreatite (leggi l'articolo), una patologia infettiva es. peritonite infettiva felina (FOTO 3) si può avere la formazione di liquidi chiamati essudati, dei fluidi acquosi ricchi di cellule infiammatorie (globuli bianchi).Anche alcuni tipi di tumore (es. linfoma (leggi l'articolo)) possono determinare la formazione di un essudato ricco di cellule tumorali (es. linfociti, nel caso di un linfoma). - Nelle cagne e nelle gatte non sterilizzate si può sviluppare un’infezione dell’utero, caratterizzata da un accumulo di pus al suo interno, che prende il nome di piometra. FOTO 3 - Dilatazione addominale in un gatto (foto a sinistra) causata dalla presenza di materiale fluido in addome (foto a destra).L’addome del gatto appare ampio e con un aspetto rotondeggiante. Le analisi citologiche e biochimiche effettuate sul fluido hanno dimostrato che si trattava di un essudato, formatosi a causa di una malattia infettiva, la peritonite infettiva felina (FIP), diagnosticata successivamente con un’analisi di laboratorio specifica (RT-qPCR). GAS IN ADDOME O NEL TRATTO GASTROENTERICO La presenza di un’elevata quantità di gas nello stomaco o nell’intestino può essere dovuta ad una torsione degli stessi organi o ad una paralisi intestinale, che non permette al cibo e al gas al loro interno di essere espulso correttamente. La presenza di gas in addome può anche derivare da una perforazione del tratto gastroenterico (solitamente ciò è dovuto ad un oggetto ingerito che perfora l’intestino) o da una perforazione della parete addominale che causa l’entrata di aria dall’esterno.In casi più rari anche un’infezione batterica a carico di alcuni organi addominali (es. vescica, cistifellea) può portare alla formazione di gas in addome. I pazienti che hanno subito una chirurgia addominale possono avere una moderata quantità di gas in addome: anche in questo caso, come per i piccoli accumuli di sangue precedentemente citati, la condizione non risulta rischiosa e si risolve spontaneamente con le adeguate cure post-operatorie. TORSIONE E CONGESTIONE DEGLI ORGANI ADDOMINALI Come già detto nel paragrafo precedente, una torsione del tratto gastroenterico può causare accumulo di gas al suo interno.La torsione può avvenire anche a carico altri organi addominali (es. milza, fegato): in questi casi il sangue può accumularsi (congestione) all’interno degli stessi organi, causando un aumento del loro volume, danneggiandone i tessuti e rischiando di causarne la rottura e determinare un sanguinamento in addome. Una patologia caratterizzata da torsione dello stomaco, con accumulo di aria al suo interno, ed eventuale torsione e congestione della milza, prende il nome di torsione/dilatazione gastrica (leggi l'articolo), una patologia che colpisce soprattutto cani di taglia grande. IPERADRENOCORTICISMO (SINDROME DI CUSHING) Una patologia presente prevalentemente nel cane, caratterizzata da un’eccessiva produzione o assunzione di steroidi (ipercortisolismo o sindrome di Cushing) (leggi l'articolo) può determinare una distensione dei muscoli dell’addome e ad un aumento di volume del fegato: entrambi questi fenomeni possono causare un aumento di volume dell’addome (FOTO 5).Questa malattia deve essere presa in considerazione ed eventualmente indagata dal vostro Medico Veterinario in presenza di alcuni segni clinici specifici (es. aumento del bere e dell’urinare, perdita del pelo) e di specifiche alterazioni agli esami del sangue. foto 5FOTO 5 e In Copertina - Cane di 11 anni affetto da sindrome di Cushing.Si noti l’addome aumentato di volume. COME FACCIO A CAPIRE SE LA DILAZIONE ADDOMINALE È UN’URGENZA PER IL MIO CANE E IL MIO GATTO? In alcuni casi la dilatazione addominale può svilupparsi velocemente e peggiorare nel giro di poche ore.In questi casi è importante notare se il cane o gatto possa aver subito un trauma o se presenti altri sintomi potenzialmente preoccupanti quali depressione del sensorio e debolezza generale, incapacità a camminare, dolore, perdita di appetito, vomito, presenza di conati o eccessiva salivazione.In questi casi è necessario contattare immediatamente il Medico Veterinario. COME SI EFFETTUA LA DIAGNOSI? Per effettuare una diagnosi corretta della patologia sottostante il Medico Veterinario, a seconda della presentazione del paziente e della successiva visita clinica, potrà richiedere alcuni esami di laboratorio (emogramma, esame biochimico ed esame delle urine) che permettano di valutare la presenza di un’infezione, una perdita di sangue e la funzionalità dei principali organi addominali.Possono risultare fondamentali degli esami strumentali (ecografia addominale, radiografia addominale e toracica) per valutare la presenza di neoformazioni, fluidi patologici o gas in addome. Successivamente potrebbero essere necessarie ulteriori analisi specifiche, quali il prelievo dei fluidi patologici (solitamente effettuato con un ago sottile), su cui effettuare un esame citologico o biochimico per poterne determinare la natura.Il prelievo viene effettuato inserendo un ago nell’addome, una procedura normalmente non rischiosa e non dolorosa, che viene effettuata con il cane e il gatto svegli.Infine, la valutazione della funzionalità del cuore, tramite un’ecografia cardiaca o un elettrocardiogramma, e di specifici esami ormonali potranno essere richiesti sulla base dei sospetti diagnostici del Medico Veterinario. QUAL È IL TRATTAMENTO PIÙ ADATTO? Per risolvere la causa dell’aumento di volume dell’addome nel cane e nel gatto è necessario intervenire sulla specifica causa scatenante. Nei casi più gravi, in cui la malattia sottostante mette a rischio la vita del cane e del gatto, può essere necessario intervenire in urgenza, attraverso cure intensive in pronto soccorso o richiedendo un intervento chirurgico urgente, come nei casi di una torsione/dilatazione gastrica o di una perforazione intestinale.In collaborazione con il Dr. Francesco Lunetta “DVM, Diplomato ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Internal Medicine - Animali da compagnia, Endocrinologia non riproduttiva, medicina interna e terapia (Malattie Metaboliche).”Prof. Federico FracassiAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

L’aumento di volume dell’addome è un evento che nel cane e nel gatto può riconoscere numerose e diverse cause.In questo articolo andremo a descrivere le principali motivazioni e come riconoscere alcuni sintomi che, associati ad un ingrandimento dell’addome, possono rappresentare un’urgenza medica. L’addome contiene al suo interno diversi organi vitali: lo stomaco, l’intestino, il fegato, la milza, la vescica, i reni, il pancreas, la prostata e l’utero. Alcune malattie a carico di questi organi possono, in certi casi, determinare un aumento di volume dell’addome. Bisogna innanzitutto ricordare che le diverse razze (soprattutto nei cani) possono avere un addome con diverso aspetto: in alcune razze è stretto e alto, in altre appare normalmente più ampio e profondo (FOTO 1).Per poter riconoscere un’eventuale dilatazione addominale è importante ricordare queste importanti differenze di razza. FOTO 1 - Un cane di razza Galgo español (levriero, a destra) e un cane Bovaro del bernese (molossoide, a sinistra).Si può notare come l’ampiezza e la profondità dell’addome sia differente tra le due razze di cani.QUALI SONO LE PRINCIPALI CAUSE DI AUMENTO DI VOLUME DELL’ADDOME? GRAVIDANZA Nel caso più ovvio di un cane o gatto femmina, non sterilizzata, in cui si instaura una gravidanza, si può notare un progressivo aumento di volume dell’addome con il passare delle settimane (FOTO 2).A meno che non sia stato possibile osservare l’avvenuto accoppiamento, cani e gatti con stile di vita prettamente outdoor possono sviluppare una gravidanza inaspettata.FOTO 2 - immagine radiografica dell’addome di una cagna in corso di gravidanza.Le frecce indicano la presenza di alcuni feti, evidenti dai profili delle ossa della colonna vertebrale e della testa.ECCESSO DI ALIMENTI, FECI O PARASSITI NEL TRATTO GASTROENTERICO Un’eccessiva alimentazione, soprattutto in cuccioli o in cani/gatti sottopeso, può causare un transitorio aumento di volume dell’addome che si risolve al termine della digestione. Un accumulo eccessivo di feci nell’intestino può, invece, essere una condizione patologica, come causa o come conseguenza di alcune patologie gastroenteriche (costipazione, megacolon (Leggi), paralisi intestinale). Un’infestazione da parte di parassiti intestinali (solitamente vermi tondi, gli ascaridi), che si sviluppa tipicamente in cuccioli non adeguatamente trattati con farmaci antiparassitari, può determinare la presenza di un addome più dilatato, evidente anche durante il digiuno (FOTO 4).FOTO 4 - addome dilatato in un cucciolo di gatto affetto da un’infestazione di ascaridi (vermi) intestinali. NEOFORMAZIONI IN ADDOME Lo sviluppo di alcuni tumori o neoformazioni negli organi addominali può portare ad un aumento del suo volume. I tumori possono essere di diverso tipo, con diverso comportamento (benigno o maligno) in base all’organo in cui esso si sviluppa e in base alla propria natura. Altri tipi di neoformazioni che si possono sviluppare in addome sono le cisti, delle strutture composte da una capsula che contiene al suo interno un materiale fluido (vedi paragrafo successivo per la natura dei fluidi). Quando queste cisti contengono del pus (fluido composto da globuli bianchi degenerati e batteri) si tratta di una reazione dovuta ad un’infezione, solitamente causata da batteri, e la neoformazione prendono il nome di ascesso. In caso un’infezione cronica (che dura da diverse settimane o mesi) o causata da parassiti, funghi e oggetti solidi che sono penetrati in addome (es. spighe vegetali) si può avere la formazione di granulomi, strutture formate da cellule infiammatorie e tessuto cicatriziale. FLUIDI IN ADDOME In alcuni casi l’addome può aumentare di volume se al suo interno si accumulano dei fluidi patologici. La natura di questi fluidi e le cause del loro accumulo possono essere varie.1) L’accumulo di sangue in addome (emoaddome) è un evento possibile in pazienti che hanno subito un trauma (un investimento, una caduta da altezza elevata) che ha causato la rottura di organi (es. milza o fegato) o di vasi sanguigni.Alcuni tumori, come l’emangiosarcoma (che origina spesso nella milza, un organo addominale estremamente ricco di sangue) possono andare incontro a rottura, anche spontanea senza che vi siano stati traumi, e causare sanguinamenti in addome.Anche l’ingestione accidentale di rodenticidi (sostanze tossiche comunemente utilizzate come esche per topi infestanti) impedisce al sangue di coagulare correttamente, determinando sanguinamenti in addome o in altre parti del corpo. Infine, pazienti che hanno subito una chirurgia addominale possono sviluppare un accumulo di sangue in addome di lieve entità e solitamente non rischioso, che si risolve spontaneamente nei giorni successivi alla chirurgia con le adeguate cure post-operatorie. - Un liquido di natura urinosa (caratterizzato dalla presenza di urina) può riversarsi in addome in seguito alla rottura delle vie urinarie (ureteri, vescica o uretra).- Un liquido di natura biliare (caratterizzato dalla presenza di bile, una sostanza prodotta dal fegato, necessaria per la digestione degli alimenti) può invece essere presente in caso di rottura della cistifellea (l’organo in cui la bile viene immagazzinata). Questi due eventi (rottura delle vie urinarie e delle vie biliari) possono altresì avvenire in seguito ad un trauma o in seguito ad un’ostruzione delle vie specifiche (presenza di calcoli urinari o biliari, tumori che ostruiscono le vie specifiche). - Alcune gravi malattie del fegato (insufficienza epatica, ipertensione epatica) o del cuore (insufficienza cardiaca) possono determinare la formazione di liquidi addominali chiamati trasudati, dei fluidi acquosi con variabili concentrazioni proteiche che originano dal circolo sanguigno.Anche altre malattie croniche es: malattia renale cronica (leggi l'articolo) o enteropatia proteino-disperdente (leggi l'articolo) possono, nei casi più gravi, portare allo sviluppo di questo tipo di fluido in addome. - Quando alcuni organi addominali sviluppano una patologia infiammatoria es. pancreatite (leggi l'articolo), una patologia infettiva es. peritonite infettiva felina (FOTO 3) si può avere la formazione di liquidi chiamati essudati, dei fluidi acquosi ricchi di cellule infiammatorie (globuli bianchi).Anche alcuni tipi di tumore (es. linfoma (leggi l'articolo)) possono determinare la formazione di un essudato ricco di cellule tumorali (es. linfociti, nel caso di un linfoma). - Nelle cagne e nelle gatte non sterilizzate si può sviluppare un’infezione dell’utero, caratterizzata da un accumulo di pus al suo interno, che prende il nome di piometra. FOTO 3 - Dilatazione addominale in un gatto (foto a sinistra) causata dalla presenza di materiale fluido in addome (foto a destra).L’addome del gatto appare ampio e con un aspetto rotondeggiante. Le analisi citologiche e biochimiche effettuate sul fluido hanno dimostrato che si trattava di un essudato, formatosi a causa di una malattia infettiva, la peritonite infettiva felina (FIP), diagnosticata successivamente con un’analisi di laboratorio specifica (RT-qPCR). GAS IN ADDOME O NEL TRATTO GASTROENTERICO La presenza di un’elevata quantità di gas nello stomaco o nell’intestino può essere dovuta ad una torsione degli stessi organi o ad una paralisi intestinale, che non permette al cibo e al gas al loro interno di essere espulso correttamente. La presenza di gas in addome può anche derivare da una perforazione del tratto gastroenterico (solitamente ciò è dovuto ad un oggetto ingerito che perfora l’intestino) o da una perforazione della parete addominale che causa l’entrata di aria dall’esterno.In casi più rari anche un’infezione batterica a carico di alcuni organi addominali (es. vescica, cistifellea) può portare alla formazione di gas in addome. I pazienti che hanno subito una chirurgia addominale possono avere una moderata quantità di gas in addome: anche in questo caso, come per i piccoli accumuli di sangue precedentemente citati, la condizione non risulta rischiosa e si risolve spontaneamente con le adeguate cure post-operatorie. TORSIONE E CONGESTIONE DEGLI ORGANI ADDOMINALI Come già detto nel paragrafo precedente, una torsione del tratto gastroenterico può causare accumulo di gas al suo interno.La torsione può avvenire anche a carico altri organi addominali (es. milza, fegato): in questi casi il sangue può accumularsi (congestione) all’interno degli stessi organi, causando un aumento del loro volume, danneggiandone i tessuti e rischiando di causarne la rottura e determinare un sanguinamento in addome. Una patologia caratterizzata da torsione dello stomaco, con accumulo di aria al suo interno, ed eventuale torsione e congestione della milza, prende il nome di torsione/dilatazione gastrica (leggi l'articolo), una patologia che colpisce soprattutto cani di taglia grande. IPERADRENOCORTICISMO (SINDROME DI CUSHING) Una patologia presente prevalentemente nel cane, caratterizzata da un’eccessiva produzione o assunzione di steroidi (ipercortisolismo o sindrome di Cushing) (leggi l'articolo) può determinare una distensione dei muscoli dell’addome e ad un aumento di volume del fegato: entrambi questi fenomeni possono causare un aumento di volume dell’addome (FOTO 5).Questa malattia deve essere presa in considerazione ed eventualmente indagata dal vostro Medico Veterinario in presenza di alcuni segni clinici specifici (es. aumento del bere e dell’urinare, perdita del pelo) e di specifiche alterazioni agli esami del sangue. foto 5FOTO 5 e In Copertina - Cane di 11 anni affetto da sindrome di Cushing.Si noti l’addome aumentato di volume. COME FACCIO A CAPIRE SE LA DILAZIONE ADDOMINALE È UN’URGENZA PER IL MIO CANE E IL MIO GATTO? In alcuni casi la dilatazione addominale può svilupparsi velocemente e peggiorare nel giro di poche ore.In questi casi è importante notare se il cane o gatto possa aver subito un trauma o se presenti altri sintomi potenzialmente preoccupanti quali depressione del sensorio e debolezza generale, incapacità a camminare, dolore, perdita di appetito, vomito, presenza di conati o eccessiva salivazione.In questi casi è necessario contattare immediatamente il Medico Veterinario. COME SI EFFETTUA LA DIAGNOSI? Per effettuare una diagnosi corretta della patologia sottostante il Medico Veterinario, a seconda della presentazione del paziente e della successiva visita clinica, potrà richiedere alcuni esami di laboratorio (emogramma, esame biochimico ed esame delle urine) che permettano di valutare la presenza di un’infezione, una perdita di sangue e la funzionalità dei principali organi addominali.Possono risultare fondamentali degli esami strumentali (ecografia addominale, radiografia addominale e toracica) per valutare la presenza di neoformazioni, fluidi patologici o gas in addome. Successivamente potrebbero essere necessarie ulteriori analisi specifiche, quali il prelievo dei fluidi patologici (solitamente effettuato con un ago sottile), su cui effettuare un esame citologico o biochimico per poterne determinare la natura.Il prelievo viene effettuato inserendo un ago nell’addome, una procedura normalmente non rischiosa e non dolorosa, che viene effettuata con il cane e il gatto svegli.Infine, la valutazione della funzionalità del cuore, tramite un’ecografia cardiaca o un elettrocardiogramma, e di specifici esami ormonali potranno essere richiesti sulla base dei sospetti diagnostici del Medico Veterinario. QUAL È IL TRATTAMENTO PIÙ ADATTO? Per risolvere la causa dell’aumento di volume dell’addome nel cane e nel gatto è necessario intervenire sulla specifica causa scatenante. Nei casi più gravi, in cui la malattia sottostante mette a rischio la vita del cane e del gatto, può essere necessario intervenire in urgenza, attraverso cure intensive in pronto soccorso o richiedendo un intervento chirurgico urgente, come nei casi di una torsione/dilatazione gastrica o di una perforazione intestinale.In collaborazione con il Dr. Francesco Lunetta “DVM, Diplomato ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Internal Medicine - Animali da compagnia, Endocrinologia non riproduttiva, medicina interna e terapia (Malattie Metaboliche).”Prof. Federico FracassiAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Un cucciolo in famiglia. I consigli del veterinario.Cari lettori vi presentiamo questo nuovo libro dedicato a chi vuole intraprendere la fantastica esperienza della convivenza con un cucciolo ed intende conoscere ed approfondire tutti gli aspetti legati sia alla scelta del cucciolo che all'alimentazione, educazione e prevenzione delle malattie.Riassume tutti i consigli e le raccomandazioni che i veterinari normalmente danno a chi porta un cucciolo alla prima visita ed anche i consigli che il veterinario darebbe se fosse consultato prima ancora di aver adottato o scelto un cucciolo.Con l'aiuto di "consigli", "tabelle" e "immagini" vengono riassunti in modo semplice alcuni argomenti di carattere scientifico.Acquista su Amazon12 Capitoli scritti da 7 Autori Tutti gli Autori sono Medici Veteterinari esperti MYLAV. Acquista su AmazonGli Autori Med. Vet., PhD, Esperto in comportamento animale riconosciuto FNOVI - Esperto in IAA: Interventi Assistiti con gli Animali - (Medicina comportamentale)Dr.ssa Maria Chiara CatalaniAutoreMed. Vet., PhD, Diploma Master Universitario II livello in Gastroenterologia ed Endoscopia digestiva, consulente nutrizionale (Clinical Nutrition)Dr. Giuseppe FebbraioAutoreMed. Vet., PhD, Specialista in Clinica dei Piccoli Animali, Diplomato EVPC, EBVS® - European Veterinary Specialist in Parasitology”Dr. Luigi VencoAutoreMed. Vet, PhD, Diplomato ECVM, EBVS® - European Specialist in Veterinary Microbiology, Professore Ordinario di Malattie Infettive degli Animali Domestici.Prof. Nicola DecaroAutoreMed. Vet., Diplomata ECAR, EBVS ® - European Veterinary Specialist in Animal Reproduction (Fisiologia e patologia della Riproduzione, Ginecologia e Andrologia del cane, del gatto e dei mammiferi non convenzionali, Neonatologia)Dr.ssa Maria Carmela PisuAutoreMed. Vet, Esperto MYLAV in GeneticaDr. Michele MarinoAutoreMed. Vet., PHD, Direttore de "Il Fatto Veterinario"Dr. Isidoro GrilloAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

La patologia da reflusso gastroesofageo definita dall’acronimo (GERD) (Gastro Esophageal Reflux Disease), è una delle patologie gastrointestinali più comuni nell’uomo, mentre nel cane e nel gatto è stata a lungo considerata rara. È solo negli ultimi anni che il reflusso gastroesofageo (GERD) viene diagnosticato con più frequenza anche nel cane e nel gatto. Il reflusso gastroesofageo consiste nel passaggio del contenuto liquido o solido presente nello stomaco attraverso l’esofago (struttura tubulare che trasporta il cibo dalla bocca allo stomaco) ed è un fenomeno normale che può verificarsi anche più volte al giorno. La mucosa dell’esofago ha infatti dei meccanismi di protezione per evitare che venga danneggiata dal contatto con il contenuto gastrico. Quando però la frequenza del reflusso aumenta l’acido gastrico e gli enzimi digestivi presenti nello stomaco danneggiano e infiammano la mucosa esofagea causando esofagite nei casi lievi e nei casi più gravi danni agli strati più profondi dell’esofago e quindi erosioni e/o ulcere o restringimenti del lume dell’esofago (stenosi). E’ in questi casi che si parla di malattia da reflusso gastroesofageo (GERD). La malattia da reflusso esofageo (GERD) è causata da un’alterazione a carico dello sfintere esofageo inferiore, una zona della muscolatura esofagea che in condizioni di normalità si contrae impedendo la risalita dei fluidi e del cibo lungo l’esofago. Quali sono le cause del reflusso gastroesofageo nel cane ? Le cause della malattia da reflusso gastroesofageo (GERD) nei cani possono essere molteplici e spesso causate dalla combinazione di più fattori. Uno sfintere esofageo inferiore debole oppure la presenza di ernia iatale (condizione patologica caratterizzata dal passaggio di una porzione dello stomaco dall'addome al torace, attraverso un foro del diaframma normalmente presente) possono determinare reflusso poiché entrambe le condizioni consentono al contenuto gastrico di refluire nell’esofago. Altre condizioni che possono causare reflusso gastroesofageo sono: vomito cronico corpi estranei esofagei condizioni anatomiche o funzionali che rallentano lo svuotamento del contenuto dello stomaco nell’intestino patologie delle vie respiratorie superiori la sindrome brachicefalica alcune procedure chirurgiche come la sterilizzazione nella cagna femmina alcuni farmaci come gli anestetici che riducono il tono dello sfintere esofageo inferiore. Quali sono i principali sintomi clinici del reflusso gastroesofageo ? I sintomi clinici dipendono dalla causa che determina il reflusso e soprattutto dalla sua gravità. Il sintomo più frequente è il rigurgito che consiste nell’eliminazione di materiale alimentare proveniente dall’esofago, che non ha raggiunto lo stomaco. Per tale motivo spesso l’animale tende a rimangiarlo, caratteristica tipica del rigurgito. Inoltre al contrario del vomito nel rigurgito l’espulsione del materiale contenuto nell’esofago è passiva, per cui non richiede sforzo o conati. Altri segni clinici che si riscontrano in corso di reflusso gastroesofageo (GERD) sono: eccessiva salivazione (ptialismo) difficoltà nel deglutire (disfagia) disagio e/o dolore durante la deglutizione irrequietezza durante il riposo soprattutto notturno masticazioni a vuoto e leccamento delle labbra. Nei casi più gravi, i cani possono iniziare a perdere peso perché non assumono più un’alimentazione adeguata o perché manifestano diminuzione dell’appetito. Possono inoltre comparire segni clinici che non riguardano l’apparato digerente, come tosse e febbre come conseguenza dell’inalazione di materiale liquido o solido (polmonite ab ingestis). Come si diagnostica il reflusso gastroesofageo ? Per la diagnosi del reflusso gastroesofageo (GERD) è importante descrivere bene al Medico Veterinario la storia clinica ed i sintomi. Per un proprietario non molto esperto può essere difficile differenziare il vomito dal rigurgito per cui può essere di grande aiuto, per il Veterinario, la visione di un video che consenta una chiara caratterizzazione del sintomo. Poiché esistono diverse patologie che causano segni simili al reflusso gastroesofageo, il Veterinario potrà richiedere esami di laboratorio e strumentali, come per esempio radiografie del torace ed ecografia addominale, utili per escludere altre cause potenzialmente responsabili dei sintomi descritti. Nella maggior parte dei cani affetti da reflusso gastroesofageo (GERD), gli esami sopra indicati risulteranno nella norma. A questo punto il veterinario potrebbe procedere con un esame endoscopico del tratto digerente che si esegue con il paziente in anestesia generale. Questo esame viene eseguito con una sonda munita di telecamera all’estremità della punta, con la quale è possibile visionare direttamente gli organi interessati, nel caso specifico cavità orale, orofaringe, esofago, stomaco al fine di valutarne le caratteristiche anatomiche ed eventuali alterazioni. Le alterazioni riscontrabili all’esame endoscopico, in corso di reflusso gastroesofageo (GERD), possono essere diverse e di grado variabile come ad esempio variazioni di colore della mucosa (aumento del rossore della mucosa tipicamente in corrispondenza del cardias che è la porzione che mette in comunicazione esofago e stomaco), presenza di materiale estraneo liquido o solido che ristagna all’interno dell’esofago, corpi estranei (quando presenti), evidenza di strie di eritema soprattutto in corrispondenza del cardias o erosioni e/o ulcere della mucosa o stenosi (restringimenti del lume).In alcuni casi, pur in presenza di esofagite e reflusso gastroesofageo (GERD) è possibile non riscontrare lesioni visibili. Quale terapia potrà prescrivere il Medico Veterinario? Generalmente il trattamento che il Medico Veterinario potrà prescrivere, sarà costituito da una combinazione tra terapia farmacologica e modulazione della dieta, terapia che può variare da paziente a paziente in base alla gravità del problema ed alla causa sottostante. In primis un consiglio è quello di ridurre la quantità del pasto serale anticipandolo quando possibile nel tardo pomeriggio; questo perché durante il riposo si ha una riduzione del tono dello sfintere esofageo inferiore fattore predisponente il reflusso e la peristalsi (contrazione muscolare che consente il movimento del contenuto presente in questo organo) normalmente rallenta. Entrambe queste condizioni favoriscono il ritorno del cibo dallo stomaco all’esofago. In alcuni pazienti può essere consigliata una dieta con un minore tenore di grassi e di fibra, che possono ritardare lo svuotamento del contenuto dello stomaco nell’intestino, ottenendo in questo modo la riduzione della pressione sullo sfintere esofageo inferiore. In presenza di lesioni erosive/ulcerative potranno essere consigliati farmaci che agiscono come barriera protettiva sulla mucosa esofagea o che riducono o inibiscono la produzione acida gastrica (H2 antagonisti o inibitori di pompa protonica). Nel caso siano presenti sintomi respiratori compatibili con polmonite ab ingestis potrà essere associata anche una terapia antibiotica. “DVM, Master di 2° livello in Gastroenterologia ed Endoscopia degli animali d’affezione (gastroenterologia, pneumologia).”Dr. Pietro RuggieroAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Le tartarughe acquatiche sono molto diffuse, le specie più comuni sono la Chrysemys picta e la Trachemys scripta scripta che, se gestite in modo corretto, possono superare i 30 anni d’età. Sono animali molto robusti e resistenti tanto da poter essere allevati da adulti in laghetti e stagni anche d’inverno. Il loro habitat in cattività non corrisponde alla classica “vaschetta di plastica”, bensì ad un acquaterrario munito di un filtro per depurare l’acqua, un ossigenatore e un sistema di termostati sia in acqua che nella porzione emersa. La parte di acqua deve essere alta più del doppio della lunghezza della tartaruga e deve occupare circa 2/3 dell’acquario perché questi animali devono avere la possibilità di nuotare. La parte emersa serve per fare “basking”, con questo termine si indica il comportamento tipico delle tartarughe quando si espongono alla luce solare. Le tartarughe acquatiche sono degli animali a sangue freddo non in grado di regolare la loro temperatura corporea; è importante, quindi, che la temperatura all’interno della vasca sia mantenuta costante tra i 22°C e i 28°C durante il giorno, mentre durante la notte può essere anche di 5°C più bassa. È necessario riscaldare sia l’acqua che la parte emersa. In acqua si deve inserire un termostato per acquari che può essere in plastica oppure in vetro. In quest’ultimo caso, deve essere protetto da una rete perché gli animali potrebbero procurarsi delle ustioni e le tartarughe di grandi dimensioni potrebbero romperlo con il movimento. Nella parte emersa deve essere inserita sia una lampada in ceramica collegata ad un termostato per terrari che una lampada UV. La lampada in ceramica serve per riscaldare l’ambiente non acquatico, in questo modo gli animali non subiranno sbalzi di temperatura una volta usciti dall’acqua. La lampada UV deve sviluppare UVA e UVB e deve restare accesa per dieci ore al giorno, si consiglia di sostituire la lampada una volta all’anno. La carenza di esposizione ai raggi UVA/B, che simulano l’esposizione alla luce naturale del sole, può causare l’insorgenza di malattie metaboliche. La malattia ossea metabolica (MOM, MBD o Metabolic Bone Disease), ad esempio, è una patologia che causa demineralizzazione e ridotta calcificazione del tessuto osseo. È una patologia tipica delle tartarughe di acqua non gestite in modo corretto e si può prevenire fornendo un ambiente e un’alimentazione idonea alle necessità della specie. Per quanto riguarda l’alimentazione delle tartarughe di acqua, le tartarughe adulte sono principalmente onnivore ma da piccole preferiscono alimentarsi con una dieta carnivora. Nei primi anni di vita il cibo deve essere somministrato tutti i giorni, successivamente è possibile alimentarle tre volte a settimana. La dieta delle tartarughine di acqua deve essere varia e possiamo scegliere diversi alimenti quali: latterini, novellame di sardine e acciughe, ritagli di salmone, sgombro, trota, gamberi decongelati, mazzancolle, scampi, vongole, cozze, pezzetti di pollo e tacchino, mela, cocomero, melone, fagiolini, cicoria, radicchio, carota, lattuga e pellet per tartarughe acquatiche. Il cibo essiccato deve essere evitato perché è spesso contaminato e povero di sostanze nutritive. È possibile alimentare le tartarughe di acqua in una vasca a parte per mantenere l’acqua pulita più a lungo.In questo caso è necessario controllare anche la temperatura dell’acqua della vasca per l’alimentazione al fine di evitare sbalzi termici che potrebbero farle ammalare. “DVM, GPCert medicina e chirurgia degli animali esotici, Responsabile settore Animali non Convenzionali Mylav La Vallonea”Dr. Gustavo PicciAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

La laringe è un organo composto da diverse cartilagini, avente funzione principale di garantire il passaggio d’aria e impedire l’aspirazione di cibo e liquidi. Normalmente in fase inspiratoria la laringe aumenta il diametro glottideo tramite la contrazione dei muscoli cricoaritenoidei dorsali che abducono le cartilagini aritenoidi.Questo in termini più semplici significa che durante l'inspirazione la laringe si apre per permettere il passaggio dell'aria. I muscoli cricoaritenoidei dorsali sono innervati dal nervo laringeo caudale che rappresenta la parte terminale del nervo laringeo ricorrente, a sua volta derivante dal nervo vago. La denervazione dei muscoli cricoaritenoidei ha come principale conseguenza l’immobilità delle cartilagini aritenoidi che tendono a posizionarsi stabilmente su un piano paramediano durante tutte le fasi respiratorie (ovvero la laringe non si apre più). Nella maggior parte dei casi questo deficit motorio è progressivo e possono passare anche mesi prima che il paziente mostri segni clinici riferibili ad un diminuito diametro della glottide.Questa situazione crea sintomi ingravescenti in caso di aumentata attività fisica e/o condizioni climatiche caldo-umide innescando una serie di circoli viziosi che portano l’animale verso una crisi dispnoica potenzialmente mortale. Che cosa succede? Per vincere l’ostruzione glottidea il cane deve aumentare la profondità degli atti inspiratori creando un flusso d’aria più veloce e vorticoso in grado di causare, come prima conseguenza, iperemia ed edema della mucosa laringea con ulteriore progressiva diminuzione del diametro glottideo. L’incremento dell’attività dei muscoli intercostali e del diaframma, necessario a vincere l’ostruzione, causa un ulteriore aumento della velocità di flusso ed un collasso dinamico delle cartilagini aritenoidi sulla base dell’effetto Bernoulli. Il maggiore lavoro muscolare determina un incremento nel fabbisogno di ossigeno e un aumento della temperatura corporea, entrambe evenienze che innescano un ulteriore incremento dello sforzo inspiratorio. Questo concatenarsi di eventi ha come possibile effetto finale la formazione di un edema polmonare non cardiogeno, verosimilmente secondario alle elevate pressioni negative intratoraciche in grado di favorire la fuoriuscita di fluido dai capillari polmonari verso gli alveoli e l’interstizio. Quando posso sospettare una paralisi laringea nel cane? Sono particolarmente colpiti gli animali adulti-anziani di razze grandi-giganti; tuttavia, la paralisi laringea può essere diagnosticata a cani di qualunque taglia o età. I sintomi più frequentemente riscontrati in corso di paralisi laringea si verificano durante l’attività fisica o condizioni di caldo intenso e comprendono: Respiro rumoroso con stridore, con aumento dello sforzo inspiratorio Intolleranza all’esercizio fisico Intolleranza al caldo Modifiche nella sonorità dell’abbaio Nei casi più gravi la dispnea si manifesta anche a riposo, con stridore udibile anche se di minore intensità, atteggiamento ortopnoico (collo esteso, bocca aperta, commessura labiale retratta); se il cane viene portato a compiere attività fisica anche modesta può manifestare perdita di saliva, cianosi, ipertermia, fino al collasso cardiocircolatorio. Come si diagnostica? In caso di presenza dei sintomi su menzionati il consiglio è di portare il cane con urgenza dal Medico Veterinario per una visita ed eventuali indagini successive: L’auscultazione permette infatti di identificare la zona laringea come area di insorgenza del rumore respiratorio. La valutazione radiografica rappresenta un passaggio fondamentale per il corretto inquadramento della malattia. Lo studio radiografico può individuare o far escludere masse o deformazioni a livello del tratto laringeo o tracheale cervicale o toraciche che possono essere la causa della paralisi. Inoltre il rilievo di complicazioni come polmonite o megaesofago rappresentano senza dubbio un elementi negativi che devono essere valutati attentamente prima di eseguire eventuali procedure chirurgiche. La laringoscopia è la tecnica diagnostica di elezione per emettere una diagnosi di paralisi laringea. Consiste nell’ispezione della laringe eseguita con un piano anestesiologico superficiale: con questa procedura è possibile non solo valutare l’ipomobilità o l’immobilità delle cartilagini aritenoidi ma anche evidenziare i segni secondari che si associano a paralisi, quali edema ed eritema mucosali, iperplasia da contatto, presenza di saliva o materiale alimentare a contatto delle aritenoidi o nello spazio subglottideo. Con la laringoscopia è possibile evidenziare i movimenti paradossi delle cartilagini aritenoidi derivanti dal movimento passivo che il flusso d’aria fa compiere alle cartilagini aritenoidi e alle corde vocali con l’avvicinamento delle cartilagini in fase inspiratoria e il loro allontanamento in fase espiratoria. Il quadro endoscopico mostra caratteristiche peculiari in presenza di una concomitante paralisi del nervo laringeo craniale che porta a paralisi sensoriale della mucosa laringea: in questo caso la laringe e il primo tratto tracheale sono spesso quasi completamente coperti da saliva e detriti alimentari poiché l’animale non percepisce il contatto con questi elementi che causano, nell’individuo sano, la chiusura immediata della glottide e l’innescarsi del riflesso difensivo della tosse. In presenza di paralisi laringea di tipo sensoriale la prognosi è generalmente infausta per l’elevata probabilità di aspirazione, che aumenta considerevolmente dopo l’intervento di lateralizzazione aritenoidea. Qual è la terapia se il paziente non è stabile? I pazienti in grave distress respiratorio devono essere considerati come una vera emergenza ed il Medico Veterinario provvederà ad instaurare una rapida terapia di emergenza in base alla gravità della situazione con il fine di stabilizzare il paziente. Qual è la terapia se il paziente è stabile? Nei casi in cui l’animale viene portato a visita non in situazione di emergenza, la terapia per la paralisi laringea è chirurgica e consiste nella lateralizzazione unilaterale della cartilagine aritenoidea, ovvero l’abduzione permanente (allargamento verso l’esterno) di una delle due cartilagini al fine di ottenere un diametro glottideo adeguato a permettere il normale passaggio dell’aria. Tale abduzione ha come effetto secondario la diminuzione, talvolta fino alla perdita, dell’attività fonatoria. Le complicanze più gravi della lateralizzazione aritenoidea possono essere: Aspirazione di cibo: il lume glottideo viene reso stabilmente più ampio del normale per cui il rischio di aspirazione di cibo e fluidi è potenzialmente aumentato. È da tenere presente che le vie respiratorie inferiori sono protette da altri due sistemi difensivi: l’epiglottide e il riflesso della tosse. La cartilagine epiglottide ruota durante la deglutizione agendo come una sorta di ponte levatoio che si chiude proteggendo la glottide, mentre la tosse allontana piccole particelle comunque venute a contatto con la mucosa laringea. Frattura della cartilagine aritenoide per trazioni da collare o da attività fisica troppo intensa nell’immediato periodo post-operatorio. In questo caso il cane manifesterà un riacutizzarsi improvviso della sintomatologia dispnoica: per questo motivo gli animali operati non devono essere portati a passeggio con il guinzaglio ma solo con la pettorina e l’attività fisica deve essere fortemente limitata durante le prime due settimane dopo la chirurgia. Med. Vet., Dottore di Ricerca in Fisiopatologia e Clinica degli Animali da Compagnia. Specialista in Clinica e Patologia degli Animali da Compagnia - (Malattie dell’apparato respiratorio e otorinolaringoiatriche - Citopatologia generale)Dr. Davide De LorenziAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

